|
СОДЕРЖАНИЕ 1. METAPASS 2024: ПОЛЬЗОВАТЕЛЬСКИЙ ИНТЕРФЕЙС И ОСНОВНЫЕ ФУНКЦИИ СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ Рисунок 1Стартовая страница веб приложения MetaPASS 2024. Рисунок 2Основная страница ресурса MetaPASS 2024для работы с выбранной схемой биотрансформации. Рисунок 4Окно поиска активностей. Таблица 1Пополнение данных о сетях метаболизма в MetaPASS 2024. Таблица 2Список категорий активностей и цветовая кодировка целевых карт. |
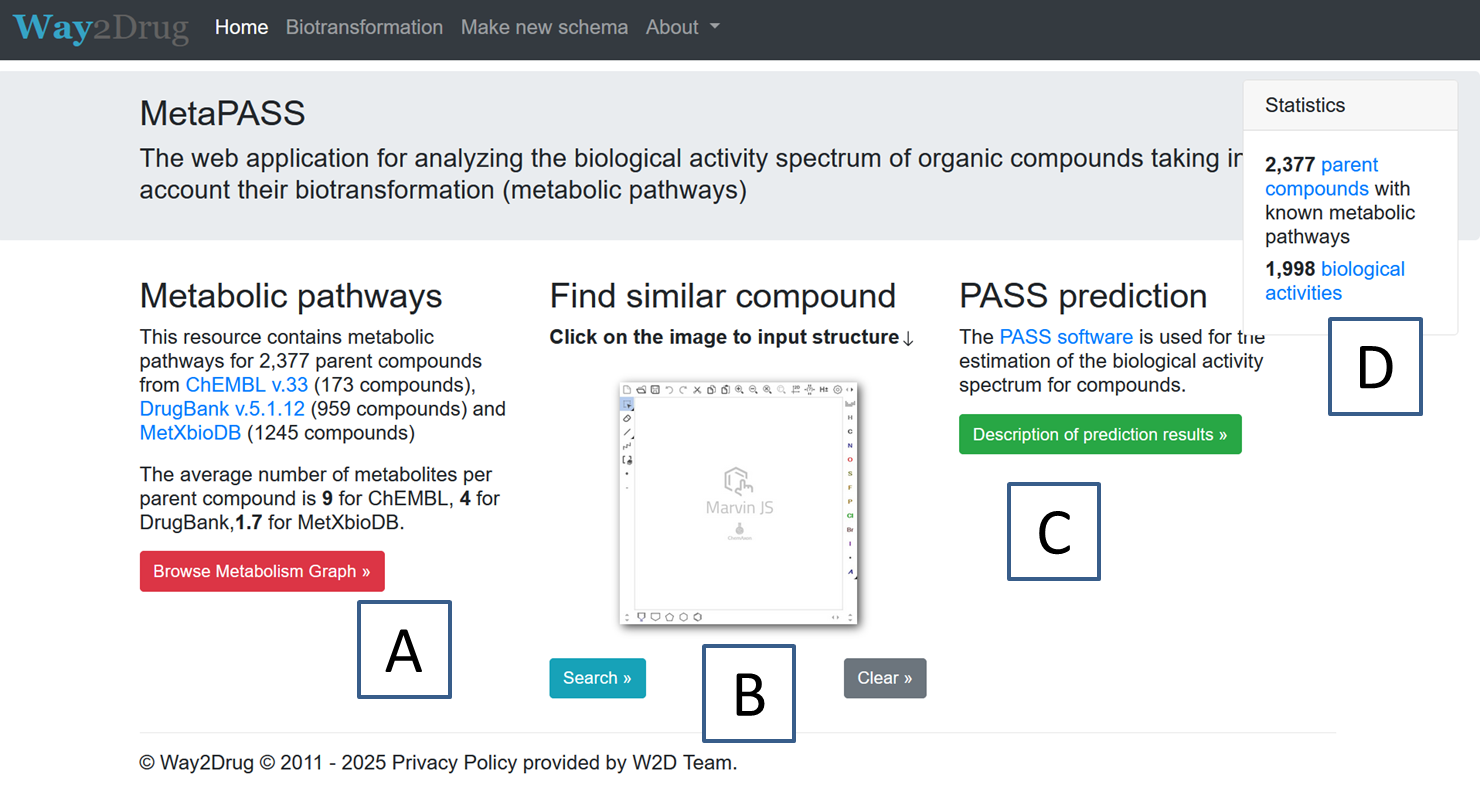
MetaPASS 2024: АНАЛИЗ ВЕРОЯТНЫХ СПЕКТРОВ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ ЛЕКАРСТВЕННО-ПОДОБНЫХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С УЧЕТОМ ИХ БИОТРАНСФОРМАЦИИ 1Научно-исследовательский институт биомедицинской химии им. В. Н. Ореховича, 119121, Москва, ул. Погодинская, 10; *e-mail: rudik_anastassia@mail.ru Ключевые слова: лекарственно-подобные органические соединения; профили биологической активности; метаболизм ксенобиотиков; цветовая карта DOI: 10.18097/BMCRM00243 ВВЕДЕНИЕ Разработка новых лекарственных препаратов – это длительный, дорогостоящий и трудоемкий процесс [1], в котором немаловажное значение имеют вычислительные методы предсказания активности химических соединений, включая анализ взаимодействия с молекулярными мишенями и оценку безопасности применения этих соединений как потенциальных лекарств [2, 3]. Изучение фармакологически активных соединений не прекращается с выходом их на рынок. Уже одобренные к применению лекарства могут быть использованы для лечения других патологий путём перепрофилирования (репозиционирования) с целью сокращения цикла разработки препарата и снижения финансовых рисков [4]. Эффективность и безопасность соединений определяется, в том числе, его метаболитами, образующимися в ходе различных реакций биотрансформации, проходящих в организме [5]. Поэтому при прогнозе спектра биологической активности (СБА) соединения важно учитывать и возможную активность его метаболитов. Для решения этой задачи ранее нами были созданы веб-сервисы MetaPASS [6], в котором содержаться известные схемы метаболизма, и MetaTox [7], который позволяет сгенерировать и оценить потенциальные метаболиты. В данной работе мы представляем новую версию сервиса – MetaPASS 2024. В числе основных изменений – добавленная возможность поиска по структурному сходству среди всех соединений из сетей метаболизма в MetaPASS 2024. Допуская, что похожие соединения метаболизируются сходным образом, можно сделать предположение о возможной биотрансформации исследуемого соединения, либо о путях его синтеза, если подобные соединения выявлены среди конечных метаболитов. Также добавлена возможность поиска соединений – потенциальных кандидатов для репозиционирования, для которых прогнозируется заданная биологическая активность. С этой целью в сервис интегрирован частичный функционал программы PASS Refined 2022, способной провести оценку 1957 наиболее важных для медицинских химиков и фармакологов видов биологической активности, прогнозируемых со средней инвариантной точностью (IAP) не хуже 0.97 [8] 1. METAPASS 2024: ПОЛЬЗОВАТЕЛЬСКИЙ ИНТЕРФЕЙС И ОСНОВНЫЕ ФУНКЦИИ Доступ к MetaPASS 2024 организован на портале Way2Drug по адресу https://www.way2drug.com/metapass/. На стартовой странице (рис. 1) доступны несколько вариантов действия пользователя. В группе «Metabolic pathways» (рис. 1А) по нажатию кнопки «Browse Metabolism Graph» пользователь может открыть список с названиями соединений, схемы метаболизма которых представлены в сервисе. При выборе конкретного соединения из списка пользователь будет перенаправлен на основную страницу ресурса со схемой биотрансформации, в которой выбранное соединение является родительским (т.е. вершиной в дереве метаболизма) и результатами предсказания модуля PASS Refined. При выборе опции меню «Biotransformation» открывается демонстрационная страница на примере биотрансформации эпирубицина. Также в группе доступны ссылки на оригинальные источники данных, загруженных в MetaPASS 2024. В группе «Find similar compound» (рис. 1B) пользователь с использование плагина Marvin JS [9] может загрузить либо нарисовать структуру интересующего его соединения и выполнить поиск похожих соединений. Таблица с результатами поиска разделена на группы родительских соединений и метаболитов. Она включает в себя структурные формулы соединений, названия и оценку подобия. В MetaPASS 2024 использованы 2 варианта метода оценки сходства по структуре соединения с использованием дескрипторов MNA и QNA. Дескрипторы MNA представляют структуру молекулы в виде бесповторного множества строк линейной нотации атомно центрированных фрагментов с расстоянием в одну и две связи от центрального атома [8]. Дескрипторы QNA представляют структуру молекулы в виде множества пар значений P и Q, рассчитанных для каждого атома молекулы на основе матрицы связности молекулярного графа и стандартных значений потенциала ионизации и сродства к электрону атомов [10]. Они описывают каждый из атомов в молекуле, и в то же время каждое значение P и Q зависит от состава и структуры всей молекулы. Для каждой пары соединений рассчитываются два значения – коэффициент сходства T(A,B) по дескрипторам MNA и коэффициент сходства F(A,B) по дескрипторам QNA по общей формуле меры сходства Жаккарда:
где N(A) и N(B) – число дескрипторов MNA или QNA для соединений A и B, n(A∩B) – мера пересечения множеств дескрипторов соединений A и B: для дескрипторов MNA n(A∩B) равно числу одинаковых дескрипторов, а для дескрипторов QNA n(A∩B) вычисляется на основе меры Хаусдорфа:
где NA≡n(A), NB≡n(B), Pa и Qa, Pb и Qb – значения P и Q дескриптора QNA атомов a и b молекул A и B соответственно. Группа «PASS prediction» содержит ссылку на ресурс PASS online и информацию об интерпретации результата прогноза биологической активности с помощью прогноза PASS (рис. 1C). В группе «Statistics» (рис. 1D) содержится информация о количестве схем метаболизма и о количестве прогнозируемых активностей. Нажав на ссылку «biological activities», можно ознакомиться со статистикой обучающей выборки модуля PASS Refined 2022, а выбрав ссылку «parent compound» – перейти на любую схему метаболизма, представленную на ресурсе. Опция меню «Make new sсhema» позволяет пользователю создать собственную схему биотрансформации.
1.1. Стандартизация схем метаболизма и пополнение базы данных ресурса Источником информации о протекающих в организме реакциях биотрансформации для MetaPASS 2024 были базы данных ChEMBL v.33 [11], DrugBank v.5.1.12 [12] и MetXBioDB v.1 [13]. Описание данных в этих базах не унифицировано и не всегда удобно для анализа всей сети метаболизма. Например, в DrugBank нельзя увидеть структурные формулы для всего дерева метаболизма на одной странице, так как необходимо переходить в карточки описания конкретной реакции биотрансформации. В MetXBioDB присутствуют только отдельные схемы метаболизма в виде табличного описания реакций биотрансформации. Экстрагированные данные были приведены к единому формату представления в виде направленного графа, где узлами являются изображения структурных формул соединений и их непосредственных метаболитов. Также по сравнению с предыдущей версией MetaPASS увеличены число и размер депонированных сетей метаболизма (табл. 1).
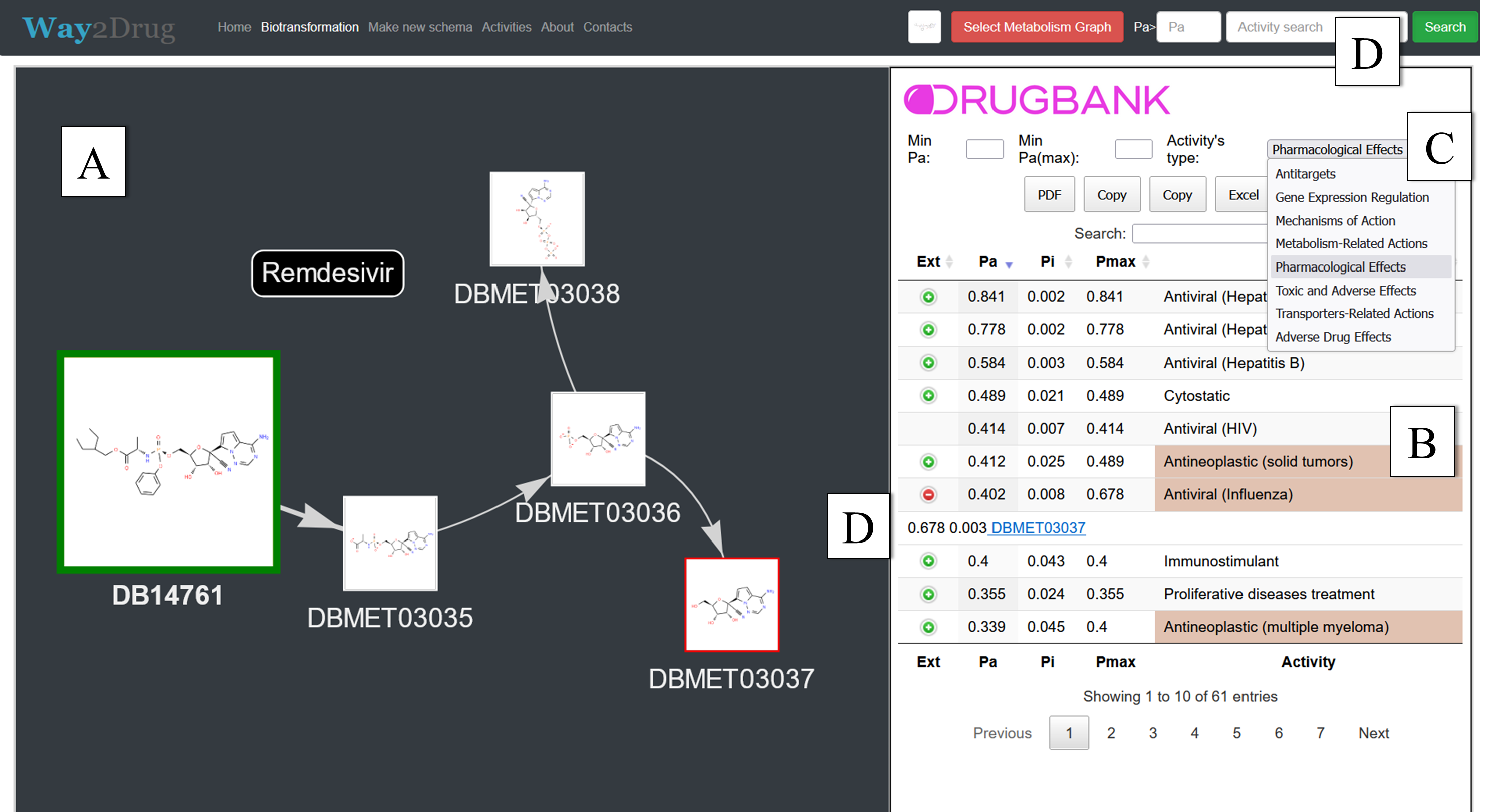
1.2. Работа со схемой биотрансформации на MetaPASS 2024 Основная страница (рис. 2) ресурса для работы с выбранной схемой биотрансформации разделена на 2 части. В левой представлена собственно сеть метаболизма (рис. 2A), в правой части – агрегированный прогноз СБА (рис. 2B) для выбранного на схеме соединения (включая метаболиты), распределённый по категориям (рис. 2C). Если биологическая активность предсказана для метаболита с бо́льшим значением Pa, чем для исходного соединения, то строка с прогнозом для данной активности окрашивается в коричневый цвет (при Pa>Pi для исходного соединения) или в серый (при Pa<Pi для исходного соединения).
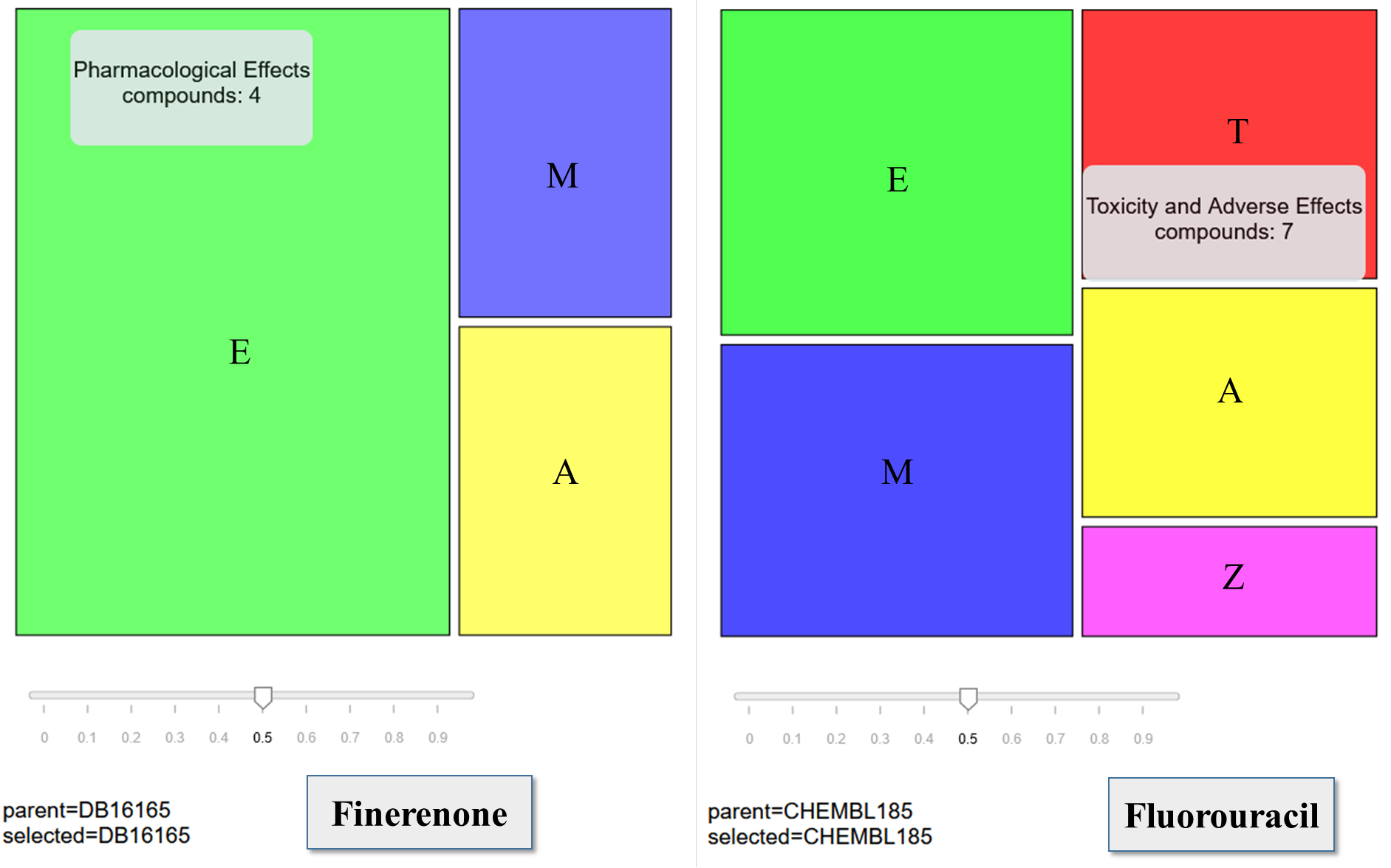
Для каждого вида биологической активности в СБА приводятся две величины: Pa (вероятность «быть активным») и Pi (вероятность «быть неактивным»), которые оценивают принадлежность прогнозируемого соединения к нечетким классам активных и неактивных соединений соответственно. Значение Pa_max определяется как максимальное значение из величин Pa, рассчитанных и для выбранного соединения, и для его метаболитов. В рамках прогноза СБА отдельные виды активности собраны в 7 категорий (табл. 2). Категории E и M включают активности, которые определяют возможности фармакотерапевтического применения биологически активных соединений. Категории T и A включают активности, которые ограничивают возможности применения фармакологических веществ в медицине. Категории Z, G и C включают активности, которые в зависимости от контекста могут способствовать проявлению соединением или его метаболитом как положительных, так и отрицательных эффектов в организме человека. Одна и та же биологическая активность может входить в две и более категории. Например, активность «Dopamine uptake inhibitor» входит в категорию M (молекулярные механизмы действия), поскольку ингибирование обратного захвата дофамина является механизмом действия ряда лекарственных препаратов, используемых для лечения депрессии [14]. Кроме того, эта же активность входит в категорию C (влияние на белки-транспортёры), поскольку такой механизм действия подразумевает подавление активности белка-транспортёра, и в категорию A (нежелательные мишени) [15], так как блокада транспортёра дофамина ассоциирована с возникновением привыкания к лекарственному препарату и поэтому во многих случаях нежелательна. В MetaPASS 2024 добавлена агрегация прогноза СБА любого соединения и его метаболитов с использованием цветовых карт, реализованных с помощью JavaScript-библиотеки Data-Driven Documents, D3.js [16]. Цветовые карты дают возможность отобразить количественные характеристики категорий активности в спрогнозированном СБА в виде соответствующих им прямоугольников [17] (рис. 3). Площадь этих прямоугольников пропорциональна количеству соединений в схеме метаболизма, для которых была предсказана хотя бы одна активность из соответствующей категории. Соответствие цветов категориям представлено в таблице 2.
Интенсивность окраски прямоугольников пропорциональна среднему значению разности Pa-Pi оценок вероятностей быть активным (Pa) и быть неактивным (Pi) в соответствующей категории СБА. Если конкретная активность была предсказана для нескольких структур, то перед усреднением берут максимальное значение Pa-Pi по этой активности. Например, в категории A с порогом Pa-Pi > 0 было предсказано две активности: A1 и A2. При этом A1 была предсказана для структур X1 и X2, с Pa-Pi, равными 0.3 и 0.5 соответственно. Активность A2 была предсказана для одного соединения с Pa-Pi, равным 0.5. При расчете сначала берут максимум по A1, который равен 0.5, а затем проводят усреднение по A1 и A2. Итоговую оценка (0.5) используют как меру интенсивности окраски прямоугольника, соответствующего категории A. Цветовые карты могут быть построены как для исходного соединения (для всей схемы метаболических превращений), так и для любого выбранного метаболита (с учетом его возможных метаболических превращений), что позволяет увидеть изменения СБА в ходе метаболизма. На рисунке 3 представлен пример цветовой карты СБА для двух соединенийфинеренона (антагонист минералокортикоидных рецепторов для лечения хронической болезни почек, связанной с диабетом 2 типа [18]) и фторурацила (противоопухолевый препарат [19]). Для обоих соединений в MetaPASS содержатся схемы метаболизма, включающие девять метаболитов. При этом цветовые карты при одном пороге (Pa-Pi >0.5) существенно отличаются (рис. 3). Для финеренона у всех соединений из метаболической сети в спрогнозированном СБА не выявлено активностей, связанных с токсичностью. У фторурацила, напротив, таких метаболитов значительное количество, что согласуется с литературными данными, в которых изучается роль метаболитов в различных видах токсичности фторурацила [19]. Таким образом, цветовая карта СБА позволяет провести предварительную оценку безопасности исследуемых лекарственных средств.
Пользователь может регулировать отображение на карте результатов прогноза по значению Pa-Pi, при этом карта динамически перестраивается. Также можно сохранить результаты прогноза в формате TSV по отдельной категории активностей, нажав на соответствующую область. Например, в таблице 3 представлены результаты прогноза фармакологических эффектов для финеренона при выбранном пороге Pa-Pi> 0.5.
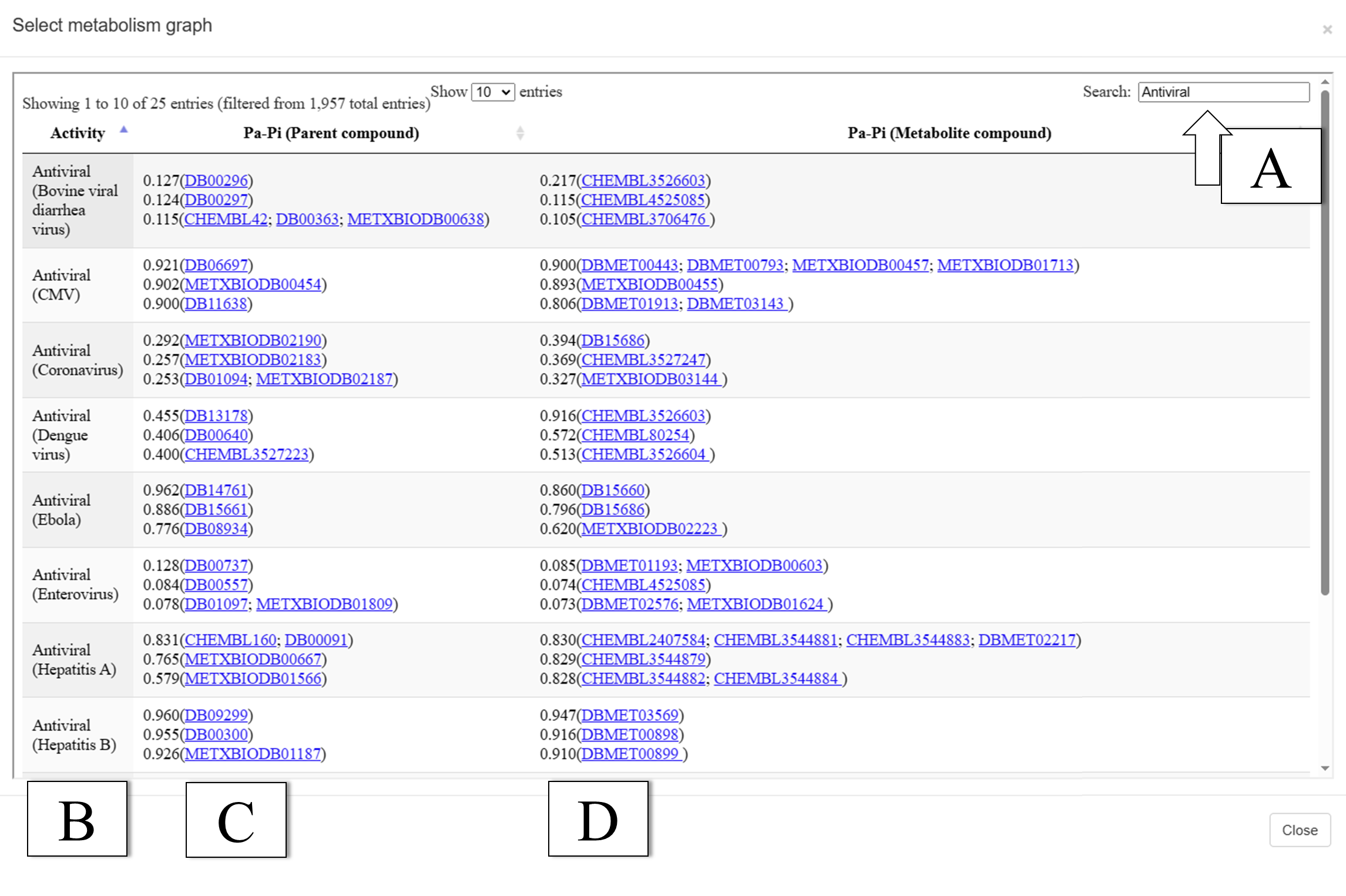
Как видно из приведенных в таблице 3 данных, активность «Urologic disorders treatment» с порогом Pa-Pi>0.5 прогнозируется только для одного метаболита, но не прогнозируется для исходного соединения, хотя финеренон используется для лечения хронической болезни почек. В данном случае учет прогноза метаболитов позволил выявить целевую активность. Чтобы проанализировать прогноз данной активности у финеренона и у всех его метаболитов из метаболической сети, нужно набрать «Urologic disorders treatment» в поле поиска в правом верхнем углу страницы (рис. 2D) и выбрать порог для Pa. После нажатия кнопки «Search» идентификаторы структур, для которых значения Pa удовлетворяют выбранному порогу, выделяются зелеными прямоугольниками со значения Pa. Также можно раскрыть список прогноза конкретной активности (кнопка в колонке «Exp») и выбрать интересующую структуру, которая будет обозначена красной рамкой на сети метаболизма. 1.3. Пример использования MetaPASS 2024 для репозиционирования лекарств Для перепрофилирования разрешенных к медицинскому применению лекарственных средств в MetaPASS 2024 появилась возможность анализа списка наиболее перспективных согласно прогнозу соединений. Нажав на кнопку «Activity», пользователь получает список названий биологической активности (рис 4, B), список значений Pa-Pi и идентифкаторов относящихся к ним структур родительских соединений (рис 4, C) и структур метаболитов (рис. 4, D). В верхнем правом углу есть строка поиска, позволяющая найти интересующую исследователя активность (рис 4, A). Например, введя «SARS» в строку поиска, можно увидеть результаты, приведенные в таблице 4.
Для активности «Antiviral (SARS coronavirus)» в таблице присутствуют идентификаторы следующих исходных соединений: нарингенин (METXBIODB02190), 7- гидроксифлаванон (METXBIODB02183), гесперетин (DB01094, METXBIODB02187) и идентификаторы метаболитов следующих соединений: ремдесивир (DB15686), амиодарон (CHEMBL3527247), кверцитрин (METXBIODB03144). Кроме ремдесивира, остальные соединения отсутствуют в обучающей выборке PASS Refined 2022, как обладающие активностью «Antiviral (SARS coronavirus)». Тем не менее, нарингенин, гесперетин, амиодарон, согласно литературе [20-22], могут быть рассмотрены как потенциальные препараты для терапии COVID-19. Кверцитрин под действием кишечной микробиоты может быть превращён в кверцитин [23], который, в свою очередь, исследуется в качестве возможного средства для лечения COVID-19 [24]. ЗАКЛЮЧЕНИЕ Новый функционал в MetaPASS 2024 расширяет возможности его применения в различных областях фармацевтических исследований и разработок, включая репозиционирование разрешенных к медицинскому применению лекарственных средств, оптимизацию профиля биологической активности новых фармацевтических агентов и оценку безопасности исследуемых лекарственных средств. СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ Данная работа не содержит каких-либо исследований с использованием людей и животных в качестве объектов. ФИНАНСИРОВАНИЕ Работа выполнена в рамках Программы фундаментальных научных исследований в Российской Федерации на долгосрочный период (2021 - 2030 годы) (№ 122030100170-5). КОНФЛИКТ ИНТЕРЕСОВ Авторы заявляют об отсутствии конфликта интересов ЛИТЕРАТУРА
|