|
СОДЕРЖАНИЕ 1. ОРГАНИЧЕСКИЕ СИСТЕМЫ ДОСТАВКИ В ГЕННОЙ ТЕРАПИИ 2. ПОДХОДЫ К ВЫБОРУ СИСТЕМ ДОСТАВКИ СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ Рисунок 2Классификация невирусных наноносителей в генной терапии Рисунок 3Примеры структур катионных липидов Рисунок 4Примеры структур анионных липидов Рисунок 5Примеры структур нейтрально заряженных липидов Рисунок 6Примеры структур ионизируемых липидов Рисунок 7Изображение фрагментов разветвленной и линейной структур PEI |
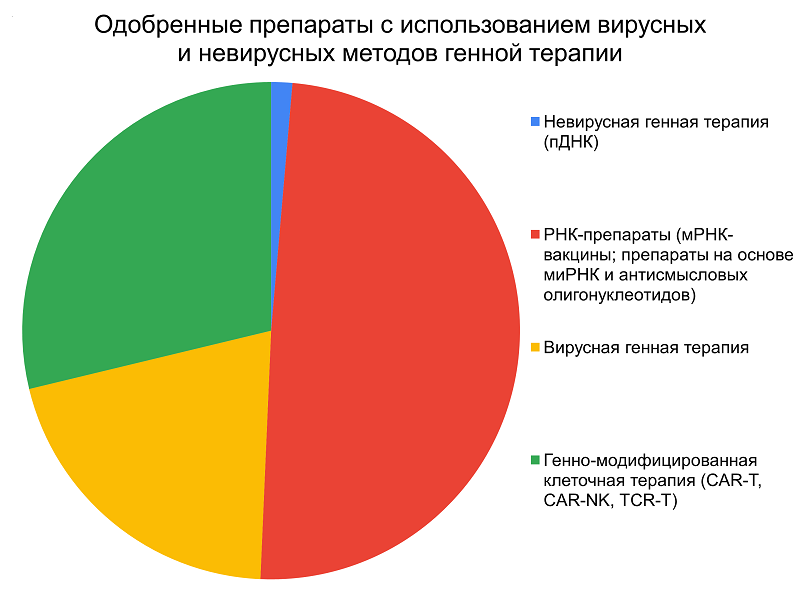
СОВРЕМЕННЫЕ МАТЕРИАЛЫ ДЛЯ НЕВИРУСНЫХ СИСТЕМ ДОСТАВКИ В ГЕННОЙ ТЕРАПИИ 1Центр регенеративной медицины, Медицинский научно-образовательный институт, Московский государственный университет имени М.В. Ломоносова, 119234, Москва, ул. Ленинские Горы, 1; *e-mail: arina.radnaeva05@gmail.com Ключевые слова: генная терапия; вектор; невирусные системы доставки; липидный вектор; поликатионный вектор DOI: 10.18097/BMCRM00287 ВВЕДЕНИЕ Системы доставки генетического материала (векторы) можно классифицировать на две группы: вирусные и невирусные. За последние десятилетия в клинических исследованиях с использованием генной терапии большинство векторных систем представлены вирусными конструкциями. На данный момент в мире зарегистрировано 66 генотерапевтических препаратов (включая препараты на основе ДНК, РНК и генно-модифицированных клеток). При этом использование незащищенных («голых») нуклеиновых кислот, за редким исключением (Неоваскулген, Collategene), не нашло широкого применения в клинической практике. Среди генотерапевтических препаратов лекарственные средства на основе вирусных векторов составляют существенную долю, что мы можем наблюдать на диаграмме (рис. 1), отражающей процентное распределение одобренных генотерапевтических препаратов по состоянию на второй квартал 2025 года [1]. Однако и невирусные системы представляют интерес.
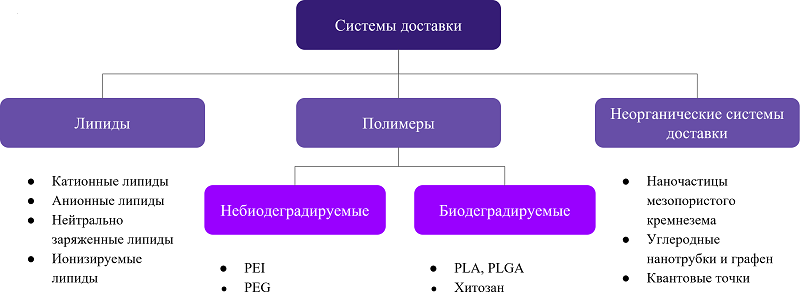
Преобладание вирусных систем над невирусными векторными конструкциями по типу плазмидной ДНК, объясняется их преимуществами – вирусные векторы обладают достаточной эффективностью трансдукции и обеспечивают высокий уровень экспрессии целевых генов. К их недостаткам относят выраженную иммуногенность, связанные с ней нежелательные реакции и иммунотоксичность, а также инсерционный мутагенез, а при местном введении – локальный воспалительный эффект [2-4]. Таким образом, существует потребность в альтернативах вирусным векторам для доставки генов с меньшим количеством нежелательных реакций. Невирусные векторы имеют лучший по сравнению с вирусными профиль безопасности, менее выраженный иммунный ответ, возможность стандартизованного и масштабного производства. Также невирусные системы доставки обладают более гибкими характеристиками нагрузки генетическим материалом по сравнению с вирусными векторами. Однако эффективность трансфекции, то есть способность невирусных векторов проникать в клетки, значительно ниже, чем у вирусных систем [5]. В поисках решения данной проблемы в последнее время значительно увеличилось количество исследований по химической модификации невирусных систем, направленной на таргетную доставку и увеличение эффективности трансфекции [6]. Также ряд исследователей обратили внимание на возможность моделирования невирусных векторов с оптимизацией пути их интернализации, так как не все механизмы вхождения являются эффективными с точки зрения дальнейшего высвобождения нуклеиновой кислоты в цитозоль и попадания в ядро [7-9]. На рисунке 2 представлена классификация современных наиболее распространенных наноносителей в генной терапии.
Основной проблемой, тормозящей развитие невирусных подходов в генной терапии (ГТ), является низкая эффективность трансфекции in vivo. Незащищенные ДНК и РНК быстро деградируют в биологических жидкостях из-за их расщепления эндонуклеазами, не накапливаются в тканях-мишенях после системного введения и не обладают специфическими механизмами для проникновения в клетки. Решение данных проблем возможно путем включения нуклеиновых кислот в специальные системы доставки. Системы для доставки нуклеиновых кислот по происхождению полимеров, на которых они основаны, можно разделить на органические и неорганические. Органические полимеры, в свою очередь, делятся на биоразлагаемые (векторы на основе липидов, пептидов, хитозана) и неразлагаемые (полиэтиленимин (PEI), полиэтиленгликоль (PEG)). Неорганические системы не способны к деградации в организме; среди них можно выделить углеродные носители (фуллерены и нанотрубки). Также существуют гибридные системы, включающие органические и неорганические полимеры [10]. При разработке лекарственного препарата с их использованием особое внимание уделяется биосовместимости веществ-компонентов. В оптимальном случае при попадании такого препарата в организм не должно наблюдаться выраженного токсического действия и иммунного ответа при его взаимодействии с клетками и тканями живого организма. Одним из важных качеств наиболее перспективных систем доставки является способность к биодеградации внутри организма. Основываясь на этих критериях, многообразие потенциальных носителей значительно сужается, что позволяет систематизировать и выявить наиболее перспективные варианты для доклинической и клинической разработки. 1. ОРГАНИЧЕСКИЕ СИСТЕМЫ ДОСТАВКИ В ГЕННОЙ ТЕРАПИИ
1.1. Липидные системы доставки
Большинство применяемых в ГТ липидов имеют в своей структуре положительно заряженные гидрофильные “головные” группы, благодаря которым они взаимодействуют с анионными фосфатными группами в составе нуклеиновых кислот. Электростатическое взаимодействие приводит к образованию липоплексов – комплексов липидов и нуклеиновых кислот. Благодаря силам Ван-дер-Ваальса и водородным связям липидные молекулы, как правило, образуют структуры в виде липосом, твердых липидных наночастиц или липидных эмульсий, способных включать в себя как гидрофильные соединения, так и гидрофобные [11]. Наиболее распространенная наноформа липидных соединений – липосомы и липидные наночастицы, в состав которых входят катионные, анионные, нейтрально заряженные и ионизированные липиды. Липидные соединения уже давно применяются в клинической практике для доставки генетического материала в клетки организма [10].
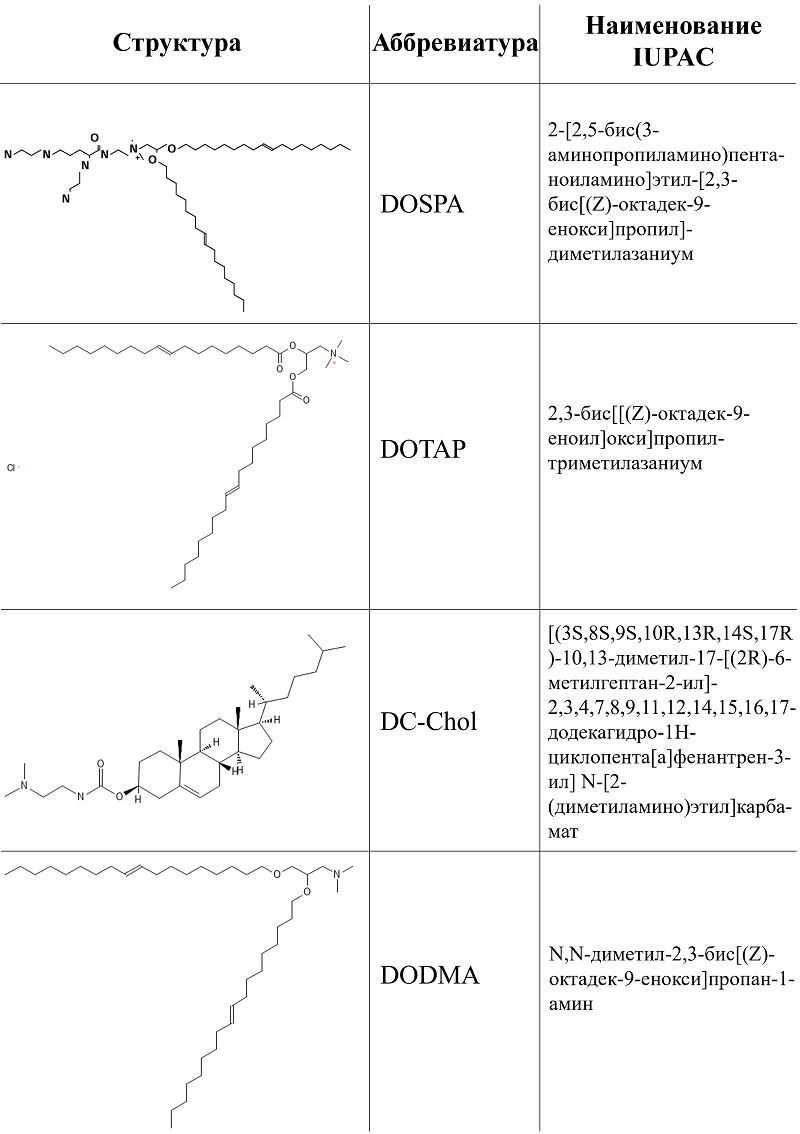
1.1.1. Катионные липиды Амфифильные молекулы катионных липидов имеют в своей структуре помимо гидрофобных хвостов и химического линкера положительно заряженные полярные головки, каждая из которых может содержать одну или несколько функциональных групп [12]. Наиболее распространенные катионные липиды для образования катионных липосом приведены на рисунке 3.
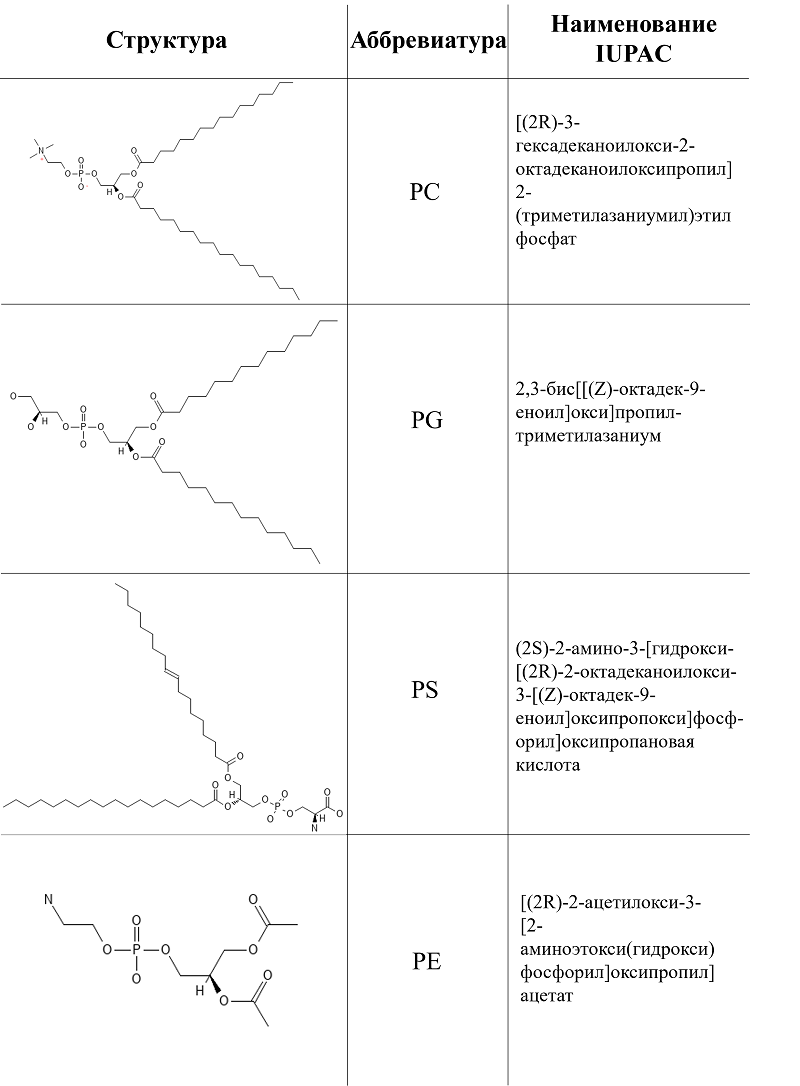
Образование комплекса липидных молекул и нуклеиновых кислот происходит за счет электростатического взаимодействия между положительными и отрицательными зарядами. Образование липоплексов только из катионных липидов, как правило, предполагает наличие избытка липидов, что приводит к накоплению положительных зарядов и более высокой эффективности захвата ДНК с увеличением интернализации комплекса в клетки. После проникновения в клетку положительный заряд липидов создает эффект “протонной помпы”: из-за связывания протонов внутри эндосомы активируется усиленная работа АТРазы в составе эндосомальной мембраны, что приводит к накоплению ионов и воды и последующему увеличению осмотического давления и разрыву эндосомы [14, 15]. Также возможен механизм нарушения целостности эндосомы путем связывания катионных липидов с липидами в составе мембраны [16]. Однако наличие положительно заряженных структурных элементов молекулы имеет и свои недостатки. Катионные липосомы имеют низкую стабильность в сыворотке, так как они способны связываться с белками плазмы крови (сывороточный альбумин, белки системы комплемента, иммуноглобулины), образуя поверхностные агрегаты. Токсичность положительно заряженных элементов молекулы еще не до конца изучена, однако известно, что катионные липосомы способны вызывать повреждение клеток и активировать провоспалительные и проапоптотические сигнальные пути [17]. По сравнению с нейтральными и отрицательно заряженными липосомами, катионные липосомы легче поглощаются фагоцитами. Это приводит к образованию активных форм кислорода и азота (супероксид и гидроксильные радикалы, оксид азота, синглетный кислород, диоксид азота и пероксинитрит), которые повреждают органеллы и способствуют повышению уровня натрия внутри клеток, что приводит к цитотоксичности и апоптозу клеток [18]. Некоторые исследования показали, что уменьшение дзета-потенциала катионных липосом приводит к уменьшению токсичности. С этой целью к структуре липосом добавляют нейтральные или цвиттерионные липиды [19, 20]. Катионные липосомы активно применяют в разработке РНК-вакцин. Например, DOTMA – четвертичный аммониевый липид – был использован для доставки мРНК во многие типы клеток и коммерциализирован как липофектин в сочетании с 1,2-диолеоил-sn-глицеро-3-фосфоэтаноламином (DOPE) [21]. Несмотря на эффективную инкапсуляцию нуклеиновых кислот и высокую эффективность трансфекции in vitro, катионные липиды обладают множеством недостатков, что создает ограничения в применении в ГТ in vivo. Высокий дзета-потенциал определяет выраженную цитотоксичность и гематологическую токсичность. Для решения данной проблемы в состав наночастиц можно включить PEG (полиэтиленгликоль); однако данная модификация может отрицательно повлиять на эффективность трансфекции и создать дополнительные проблемы с безопасностью. Повышая стабильность наночастиц и увеличивая время их циркуляции в системном кровотоке, PEGилирование создает риск развития иммунного ответа при повторном введении, приводя к выработке антител против PEG. Данные антитела ускоряют выведение наночастиц из организма и могут способствовать появлению побочных реакций из-за изменения биораспределения [25]. Другим вариантом может послужить комбинация с нейтральными липидами, однако и в данном случае необходим подбор оптимальной липидной композиции. 1.1.2. Анионные липиды Отрицательный заряд анионных липидных соединений обусловлен наличием фосфатных групп фосфолипидов. Изначально анионные липосомы не были широко распространены в практике из-за их отрицательно заряженных групп, которые отталкивают фосфатные основания нуклеиновых кислот, что делало невозможным включение генетического материала. Для решения проблемы инкапсуляции генетического материала в анионные липосомы для применения в ГТ были использованы вспомогательные элементы в виде двухвалентных катионов (например, Ca2+, Mg2+, Fe2+ и т. д.) [20, 26] или поликатионов по типу PEI и PEG [27]. Наиболее распространенные анионные липиды для образования анионных липосом приведены на рисунке 4.
Анионные липосомы обладают более выраженной стабильностью в присутствии сыворотки крови по сравнению с катионными и нейтрально заряженными липосомами, так как они меньше способствуют агрегации частиц [28, 29]. Анионный липид DPPG (16:0/16:0 PG - 3-(((2,3-дигидроксипропокси)(гидрокси)фосфорил)окси)пропан-1,2-диилдитетрадеканоат) обладает высокой температурой фазового перехода, что увеличивает жесткость мембраны частицы и препятствует ее разрушению при взаимодействии с липопротеинами и белками сыворотки крови. Однако и отрицательный заряд на поверхности частиц способен инициировать взаимодействие с сывороточными белками, что приводит к активному поглощению частиц ретикулоэндотелиальной системой и токсическим эффектам, таким как псевдоаллергический ответ. Поэтому анионные липосомы не применяются для терапии, которая предусматривает введение препарата в системный кровоток [30]. Однако по сравнению с катионными липосомами, анионные липиды показывают более низкую цитотоксичность, в основном, из-за того, что анионные липиды по составу схожи с естественными клеточными мембранами и обладают низкой иммуногенностью. Также благодаря сходству с клеточными мембранами структура анионных липосом способствуют меньшей вероятности фагоцитоза макрофагами и медленной кинетике выведения их из организма. При модификации анионных липосом поликатионными элементами они приобретают некоторых свойства катионных липосом, однако, с менее выраженной токсичностью [20]. Анионные липосомы проникают в клетку путем эндоцитоза, как и катионные липосомы, и при этом не способны избежать воздействия лизосомальных ферментов из-за отсутствия эффекта «протонной помпы». Для увеличения эффективности трансфекции можно модифицировать анионные липосомы катионами, например, Са2+. Положительно заряженные ионы способствуют более эффективному связыванию нуклеиновых кислот [31]. Модифицированные катионами анионные липосомы приобретают риск повышенной цитотоксичности в случае избытка ионов Са2+. Также анионные липосомы, сопряженные с катионами, имеют размер частиц около 500 нм, тогда как наиболее оптимальный размер для инициации клатрин-зависимого механизма эндоцитоза - около 200 нм. В связи с этим модификация анионных липосом ионами Са2+ обладает неоднозначным влиянием на эффективность трансфекции. Поэтому необходим подбор оптимальной формулы анионных липосом, сопряженных с положительно заряженными ионами, для достижения высокой эффективности не только инкапсуляции нуклеиновых кислот, но и доставки материала в клетку [13]. С точки зрения применения в клинической практике анионные липосомы имеют потенциал в разработке трансдермальных лекарственных систем. Гистологические исследования показали, что анионные липосомы эффективнее, чем катионные липосомы, диффундируют в дерму и волосяные фолликулы и проявляют менее выраженный раздражающий эффект. Однако из-за отрицательного заряда добиться эффективного включения генетического материала и трансфекции с использованием немодифицированных анионных липосом не удается [30, 32].
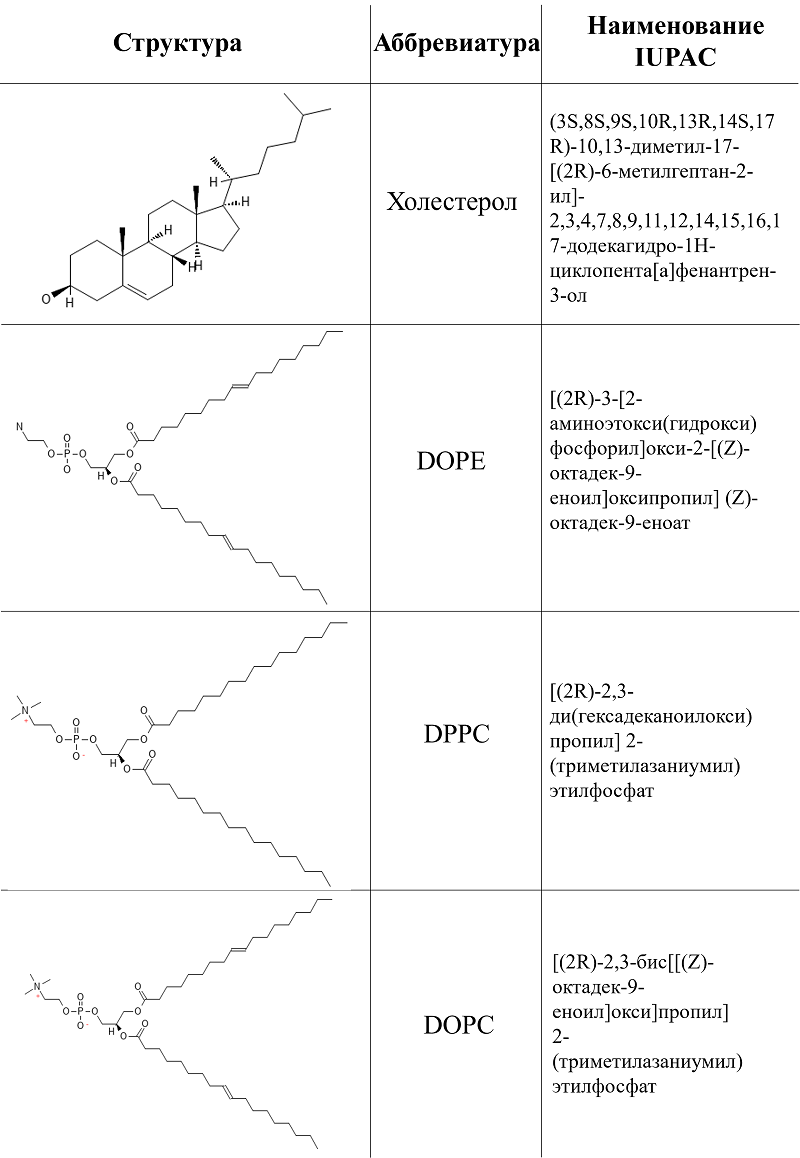
1.1.3. Электронейтральные и цвиттерионные липиды Электронейтральные и цвиттерионные липиды имеют постоянный нейтральный заряд, поэтому их основной функцией является стабилизация структуры липосом и липидных наночастиц. К этой группе относятся фосфатидилхолин, холестерин и EPC (нейтрально заряженные); DSPE (1,2-дистеароил-sn-глицеро-3-фосфоэтаноламин), DPPC (1,2-дипальмитоил-sn-глицеро-3-фосфохолин) и DOPE (1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин) (цвиттерионные). Наиболее распространенные электронейтральные липиды в составе липосом приведены на рисунке 5.
Для электронейтральных липидов сохраняется проблема инкапсуляции генетического материала: для переноса ДНК в составе частиц все еще необходима модификация катионными элементами. Нейтральные липосомы имеют преимущества в виде низкой токсичности, поскольку они не предрасположены к взаимодействию с белками сыворотки крови. Благодаря нейтральному заряду частицы могут длительное время находиться в организме, однако этот тип липосом может стохастически высвобождать свое содержимое в системном кровотоке [30]. Электронейтральные липиды используют в основном для модификаций катионных и анионных липосом в качестве линкеров в составе молекул или в качестве элементов для улучшения проникновения через мембрану клетки. Данная особенность связана со способностью цвиттерионных липидов принимать гексагональную форму при взаимодействии с клеточной мембраной (либо другими отрицательно заряженными липидами), по сути, переход из ламеллярной структуры в неламеллярную, что способствует эндоцитозу и диссоциации нуклеиновой кислоты из липоплекса, облегчая высвобождение в цитоплазму [33]. В некоторых случаях модификация цвиттерионными липидами помогает избежать стандартный путь эндоцитоза в клетки с последующей деградацией под действием лизосомальных ферментов. Липосомы, состоящие из нейтрально заряженного липида DOPE и катионного липида DOTAP, демонстрируют прямое слияние с клеточной мембраной в течение нескольких минут после контакта, что обеспечивает эффективную доставку молекулярного груза в цитоплазму клеток независимо от размера данного груза [34]. Однако существует проблема парадоксального распределения электронейтральных липидов в составе липосомы в комбинации с другими типами липидов. Молекулы цвиттерионных липидов в составе липосом обладают отрицательной кривизной, что объясняет их распределение на внутренней стороне липосомы. Такое распределение может, наоборот, увеличить энергию активации для слияния липосомы с мембраной клетки, то есть служить препятствием для данного процесса [35]. Реже сами липосомы из электронейтральных липидов модифицируют таргетными системами [36]. Нейтральный заряд облегчает внесение большинства таргетных систем, например, для доставки в опухолевые новообразования. Цвиттерионные липиды могут улучшать свойства других липидных наночастиц – увеличивать их стабильность, эффективность доставки и оптимизировать биораспределение. Например, в разработанной вакцине мРНК-1273 против COVID-19 от компании «Moderna» (США) один из ключевых компонентов липидного состава наночастиц – DPPC (1,2-дипальмитоил-sn-глицеро-3-фосфохолин). Данный фосфолипид содержит полностью насыщенные цепи, благодаря которым он создает упорядоченные липидные домены, помогающие создавать сплошную бислойную структуру для защиты мРНК от нуклеаз [37]. Также в вакцине мРНК-1273 от «Moderna» в составе липидных наночастиц содержится электронейтральный холестерол для поддержания текучести мембраны и предотвращения агрегации липидных частиц. Холестерин модулирует фазовый переход при смене температур, что позволяет хранить вакцину при -20°C, что а не при -80°C, что необходимо для некоторых препаратов [20]. В вакцине BNT162b2 против COVID-19 компании «Pfizer-BioNTech» (Германия) фосфолипид DSPC (1,2-дистеароил-sn-глицеро-3-фосфохолин) также благодаря насыщенным цепям обеспечивает стабильность липидного бислоя в составе наночастиц, а холестерин играет роль в текучести и механической прочности липидной мембраны и снижает проницаемость для воды, защищая инкапсулированную молекулу РНК [38]. Модификация липидных наночастиц холестерином или его производными может влияет на таргентность полученной системы. Липидные наночастицы, содержащие олеат холестерина, демонстрируют более высокую селективность в отношении эндотелиальных клеток сосудов печени нежели самих гепатоцитов [39]. Окислительные модификации холестеринового хвоста также позволяют липидным наночастицам накапливаться преимущественно в эндотелиальных клетках и клетках Купфера, но не в самих гепатоцитах [40]. Цвиттерионные липиды в основном применяются как вспомогательные соединения для стабилизации липидной оболочки в наночастицах и для облегчения эндоцитоза благодаря схожими с липидами мембраны клетки структурными свойствами. Однако для инкапсуляции нуклеиновых кислот нейтральные липиды не могут быть применены «в самостоятельном виде», для этого необходима модификация катионными липидами. В итоге все еще наблюдается сохранение токсичности, а для увеличения стабильности липидных векторов с цвиттерионными липидами и увеличения эффективности доставки нуклеиновых кислот необходима оптимизация липидных композиций. До сих пор для in vitro экспериментов остается популярным способ трансфекции с использованием Липофектина – смеси катионного липида DOTMA (1,2-диолеоилокси-3-(триметиламмонио) пропан) и нейтрального липида DOPE (1,2-диолеоил-sn-глицеро-3-фосфоэтаноламин) либо другой современной вариации данной липидной смеси [41]. Однако при введении в организм наличие постоянного заряда у данной системы доставки определяет уже упомянутое неприемлемое для клинических испытаний токсическое воздействие, неспецифическое связывание с внеклеточными и клеточными компонентами и короткий период полувыведения. При попытке введения в состав липидной смеси PEG, который обволакивал заряженные липидные наночастицы, удалось добиться улучшения параметров биораспределения и продлить период полувыведения. Однако при избытке PEG понижается эффективность трансфекции и нарушается оптимальное распределение в клетке [42].
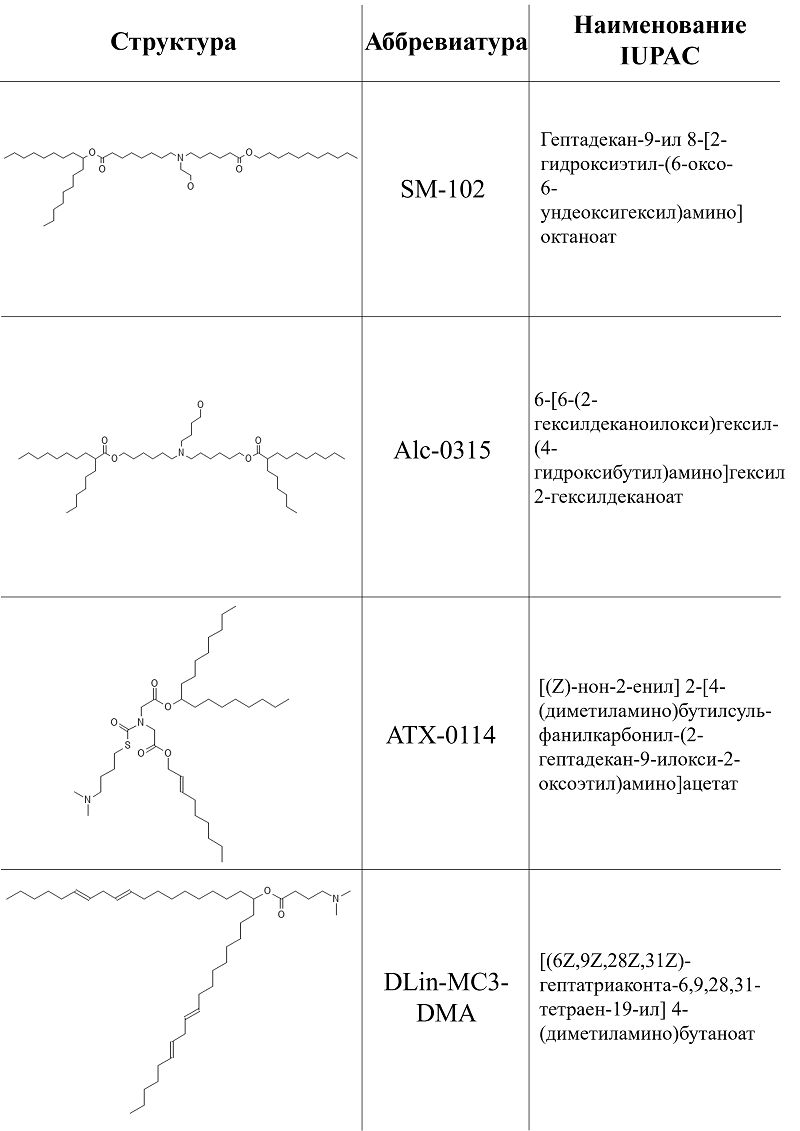
1.1.4. Ионизируемые липиды Самым перспективными системами доставки нуклеиновых кислот на данный момент среди липидных соединений являются ионизированные липиды. Они представляют собой катионные липиды, в которых аммониевый фрагмент заменен на титруемый, в результате чего заряд данных липидов определяется pKa соединения и pH среды [43]. Структуры наиболее распространенных ионизируемых липидов приведены на рисунке 6.
Самые первые исследования in vivo на приматах с синтезированными ионизируемыми липидами первого поколения (DLin-DMA (1,2-дилинолейл-N,N-диметил-3-аминопропан)) были проведены в 2006 году [45]. А уже в 2018 году FDA и EMA был одобрен первый препарат на основе интерференционных олигонуклеотидов и первый препарат с ионизированным липидом в составе Патисиран (коммерческое название Onpattro) [46]. В вышеупоминавшейся вакцине мРНК-1273 против COVID-19 от компании «Moderna» основным компонентом липидного носителя является ионизируемый липид SM-102 (гептадекан-9-ил 8-((2-гидроксиэтил)(6-оксо-6-(ундецилокси)гексил)амино)октаноат), который обеспечивает эффективную упаковку молекулы РНК. Аналогичную функцию выполняет ионизируемый липид ALC-0315 ((4-гидроксибутил)азанедиил)бис(гексан-6,1-диил)бис(2-гексилдеканоат) в составе вакцины BNT162b2 против COVID-19 компании «Pfizer-BioNTech». Однако, согласно данным молекулярной динамики, более объемная головная группа молекулы липида ALC-0315 по сравнению с липидом SM-102 снижает плотность упаковки [38]. Механизм сборки липидных наночастиц на основе ионизированных липидов с включенной в них нуклеиновой кислотой и механизм дальнейшей трансфекции заключаются в следующем [44, 47]:
Один из самых важных этапов трансфекции – высвобождение нуклеиновой кислоты из эндосомы для последующей реализации генетической информации. Клеточные исследования с ионизированными липидными наночастицами с использованием электронной и конфокальной микроскопии показали, что в цитозоль из эндосомы при доставке с использованием ионизированного липида DLin-MC3-DMA (MC3) высвобождается только 1-2% меченых золотом или флуоресцентными метками миРНК [51]. Gilleron и соавт. также описали особенности созревания эндосомы, анализируя наличие специфических маркеров [51]. В результате трансфекции ионизируемыми липидными наночастицами наблюдалась задержка созревания эндосомы и образование гибридного эндосомального компартмента, несущего как ранние маркеры (EE1, рабанкирин-5), так и поздние маркеры (LAMP1) [51]. Однако данные методы прямой визуализации миРНК оптимизированы для липоплексов (липидных наночастиц с положительно заряженными липидами в составе) и не совсем применимы для ионизируемых липидных частиц, возможно, из-за низкой нагрузочной способности последних по сравнению с крупными липоплексами. Но и в других исследованиях при оценке косвенных индикаторов - рекрутирование белков галектинов (Gal8 и Gal9 - белки, рекрутирующие поврежденные эндосомы) - фактическая цитозольная доставка миРНК составляет менее 5% [50, 52]. При попытке внесения в клетки мРНК, более крупной молекулы по сравнению с миРНК, в составе липидных наночастиц на основе ионизируемых липидов количество высвобожденной из эндосомального компартмента нуклеиновой кислоты снизилось до 1% [53]. Ионизируемые липиды в составе липидных наночастиц остаются одними из самых перспективных композиций для невирусной генной терапии. Однако и у данного вида липидных соединений все еще сохраняется риск токсичности из-за положительного заряда ионизируемых наночастиц, даже если он не постоянный [54]. Среди разрабатываемых решений для уменьшения токсичности обычных ионизируемых липидов одним из самых успешных является их замена на гликолипиды трегалозы, которые расщепляются на нетоксичные метаболиты после доставки своего «груза». Эти модифицированные липидые наночастицы (LNP S050L) продемонстрировали значительно более низкую токсичность для различных органов при сохранении эквивалентной иммуногенности [25]. Также предлагается оптимизация липидных молекул с целью изменения кинетики гидролиза, в результате чего липиды расщепляются в организме быстрее с образованием нетоксичных метаболитов [55]. Однако такая оптимизация может уменьшить эффективность доставки генетического материала. Для решения проблемы с неблагоприятной ионизацией липидов необходима структурная модификация – изменение pKa молекулы до оптимальных значений, позволяющих липидным носителям высвобождать нуклеиновые кислоты и не оказывать токсическое воздействие на мембраны клетки [56]. Липидные системы доставки хоть и обладают многообещающими возможностями для ГТ, их применение в клинике все еще ограничено токсичностью и преимущественным накоплением в печени. Но, несмотря на то, что их безопасность требует тщательного изучения, появляются инновационные подходы, позволяющие решить эти проблемы:
1.2. Системы доставки на основе катионных полимеров 1.2.1. Небиодеградируемые полимеры Несмотря на относительно несложный синтез липидных соединений, применение некоторых из них ограничено достаточно выраженной токсичностью. Альтернативным вариантом систем доставки могут служить катионные полимеры. Данная группа веществ обладает большей стабильностью и структурной пластичностью по сравнению с липидами. Катионные полимерные соединения для сборки комплекса с отрицательно заряженной молекулой ДНК положительно заряженным полимером (полиплексов) можно разделить на две группы: биодеградируемые природные полимеры и небиодеградируемые синтетические полимеры.
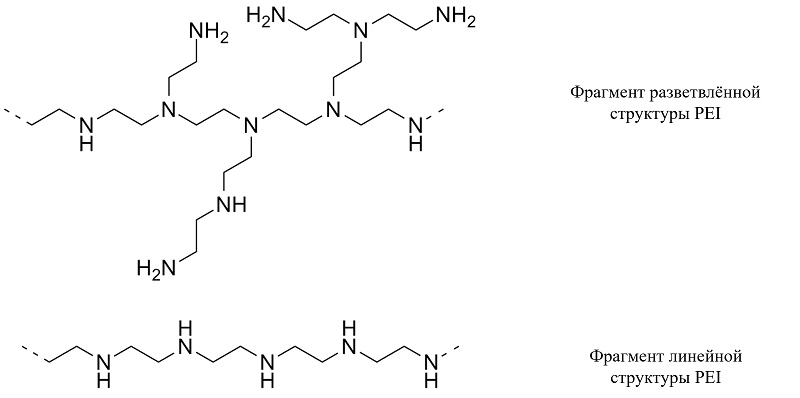
1.2.1.1. Полиэтиленимин (PEI) PEI был первым поликатионным полимером, синтезированным как в линейной, так и в разветвленной формах для ГТ еще в 1995 году. Он имеет уникальное расположение аминогрупп на основной цепи полимерной цепи, позволяющее только частичное протонирование в физиологическом диапазоне pH. PEI существует в двух различных химических структурах (рис. 7), а именно в разветвленной (BPEI) и линейной (LPEI), которые предпочтительно использовать при высокой молекулярной массе (HMW) 25 кДа и 22 кДа соответственно. В то время как BPEI содержит различные первичные, вторичные и третичные амины, LPEI содержит только вторичные амины [60].
После конденсации генетического материала с помощью PEI образуются очень стабильные при комнатной температуре полиплексы, которые также можно подвергать длительной заморозке. Механизм проникновения в клетки полиплексов на основе PEI в основном клатрин-зависимый, так как частицы имеют размер в диапазоне от 60 нм до 200 нм. По такому механизму поглощенные клеткой наночастицы направляются в эндо-/ лизосомальные компартменты, что уменьшает эффективность трансфекции из-за разрушения частиц лизосомальными ферментами. Однако присутствие заряженного PEI вызывает осмотический эффект (эффект «протонной губки»), вызывающий разрыв эндосом, что, как полагают, повышает эффективность доставки после трансфекции. Сегодня PEI с молекулярной массой 25 кДа является наиболее широко используемым агентом для переноса генов и «золотым стандартом» (положительным контролем) для оценки эффективности трансфекции невирусных векторов in vitro [61]. Богатая аминогруппами основа PEI позволяет легко модифицировать молекулу, что увеличивает специфичность и стабильность структуры, конъюгируя ее с лигандами и функциональными полимерами. Несмотря на то, что PEI считается вектором с высокой эффективностью трансфекции in vitro, он все же обладает недостаточной специфичностью и эффективностью трансфекции in vivo. PEI – это небиоразлагаемый полимер, который обладает цитотоксичностью. Помимо того, что токсичность тесно связана с катионными свойствами наночастиц, PEI сам имеет свойства поверхностно-активного вещества и способен разрушать целостность липидных бислойных мембран, что приводит к их истончению и эрозии. Структура, степень разветвления и молекулярная масса полимера определяют плотность катионного заряда. Высокая плотность заряда способствует конденсации нуклеиновых кислот, проникновению в клетку и выходу из эндосомы, однако, с другой стороны, высокая плотность положительного заряда вызывает разрушение клеточных компартментов и неспецифическое связывание анионных молекул [62]. Для уменьшения токсичности из-за высокой плотности положительного заряда предлагаются попытки экранирования полисахаридными соединениями, например, декстраном [63], крахмалом [64] и хитозаном [65], и экранирования гидрофобными молекулами – бетаметазоном, гидрокортизоном [66], холестерином [67], олеиновой [68] и гиалуроновой кислотами [69]. Молекула PEI не подвергается биологическому разложению, что приводит к накоплению токсичному для клеток организма поликатиона. Однако известно, что PEI с низкой молекулярной массой обладает меньшей токсичностью по сравнению с PEI с высокой молекулярной массой. Поэтому одним из подходов в уменьшении токсичности поликатиона является подбор биоразлагаемых линкеров для сшивания молекул PEI с низкой молекулярной массой для получения в конечном итоге высокомолекулярного PEI. Благодаря данному подходу удается добиться, с одной стороны, высокой плотности положительного заряда для конденсации нуклеиновых кислот, а с другой – сохранения низкой токсичности при биоразложении линкера. Также благодаря разрывам в цепи поликатиона в местах линкеров осуществляется высвобождение вектора для его дальнейшей реализации. В качестве линкеров могут быть окислительно-восстановительные элементы – сложные эфиры [70], дисульфиды [71] и карбаматы [72], и pH-чувствительные линкеры – глутаровый диальдегид [73], гидразон [74] и полиаспартаты [75]. Согласно литературным данным, на данный момент было проведено около 38 клинических испытаний с использованием препаратов на основе PEI для доставки нуклеиновых кислот. В большинстве из этих испытаний применяются местные способы введения PEI, такие как внутриопухолевое [76], внутримышечное [77], внутрибрюшинное [78] и внутрипузырное [79]. Например, BC-819 (инодифтаген викстеплазмида) представляет собой рекомбинантную плазмидную ДНК, которая направляет экспрессию сильнодействующего токсина специфично в злокачественных клетках, но не в нормальных тканях. Она была разработана с использованием гена H19, который активируется и экспрессируется на высоких уровнях только в злокачественных опухолях и активирует продукцию бактериального дифтерийного токсина в клетках раковой опухоли мочевого пузыря. BC-819 вводится непосредственно в мочевой пузырь, чтобы обеспечить максимальное местное воздействие на целевые раковые клетки мочевого пузыря. Для увеличения эффективность трансфекции образовывали комплекс плазмидной ДНК с полиэтиленимином (PEI); однако в 2020 году данные клинические исследования были остановлены из-за отсутствия эффективности [80, 81]. Еще одним примером использования данной системы стал препарат CYL-02 - пДНК, кодирующий второй подтип рецептора соматостатина (SSTR2), дезоксицитидинкиназы (DCK) и уридинмонофосфаткиназы (UMK) под контролем глюкозо-зависимого промотора. Введение этого препарата пациентам с аденокарциномой поджелудочной железы осуществлялось в комплексе с коммерчески доступным In vivo-jetPEI, однако результаты клинических исследований данного препарата пока не опубликованы [76, 82]. Из-за все еще существующей высокой токсичности и низкой биосовместимости PEI, в клинических испытаниях избегают системного введения. И ни одна из модифицированных генных терапий на основе PEI еще не получила одобрения FDA. Основываясь на последних тенденциях в области клинических исследований терапии на основе PEI, можно предположить, что проблема токсичности до сих пор не решена. Это находит свое отражение в небольшом количестве данных в литературе о продолжающихся испытаниях.
1.2.1.2. Полиэтиленгликоль (PEG) PEG является распространенным дополнительным компонентом, вносимым для модификации невирусных наносистем, предназначенных для доставки генетического материала. Применение самого полимера PEG в качестве носителя ДНК или РНК затрудняется вследствие химических свойств полимера, у которого отсутствуют положительно заряженные группы для образования комплексов с молекулами нуклеиновых кислот. Однако PEG способен улучшать свойства наночастиц на основе катионных полимеров или липидов, увеличивая их стабильность в жидкостях организма. PEG-цепи имеют гидрофильную природу, что при их присоединении к наночастицам способствует образованию гидратированного объемного облака, которое стерически препятствует взаимодействию наночастиц с соседними наночастицами или компонентами крови. (42) Так, например, PEG-липиды могут дополнительно способствовать стабильности частиц за счет уменьшения их агрегации, а некоторые модификации PEG продлевают время циркуляции в крови наночастиц за счет уменьшения клиренса, опосредованного почками и системой мононуклеарных фагоцитов [83–85]. Наконец, PEG-липиды можно использовать для конъюгирования специфических лигандов с частицей для адресной доставки. Степень этих эффектов зависит от пропорций и свойств PEG-липидов. Например, 1,2-димиристоил-рац-глицеро-3-метоксиполиэтиленгликоль-2000 (ПЭГ2000-DMG) и 1,2-дистеароил-рац-глицеро-3-метоксиполиэтиленгликоль-2000 (ПЭГ2000-DSG) являются нейтральными PEG-липидами, а длина их насыщенных алкильных цепей составляет C14 и C18 соответственно. Составы липидных наночастиц и миРНК, содержащие PEG2000-DMG, имеют более короткое время циркуляции и более высокую эффективность доставки in vivo, чем составы, содержащие PEG2000-DSG129. Это различие можно объяснить более быстрой диссоциацией PEG2000-DMG от липидных наночастиц по сравнению с PEG2000-DSG, что может способствовать клеточному поглощению и выходу из эндосом липидных наночастиц [86, 87]. В некоторых исследованиях in vitro при модификации поликатионных полимеров с помощью PEG ухудшилась стабильность частиц и увеличилась иммуногенность. Однако в исследованиях in vivo, наоборот, частицы на основе PEI, модифицированные PEG, демонстрировали более высокую стабильность, все еще вызывая иммунный ответ, но без гистологических изменений. Введение немодифицированных комплексов PEI/миРНК приводило к накоплению PEI в легких и слишком раннему высвобождению миРНК [88]. Наночастицы, модифицированные PEG, могут успешно преодолевать также и различные внеклеточные барьеры, что благоприятно при других способах введения препарата, например, через слизистую оболочку или в ткани головного мозга [42]. Как было указано ранее, включение в состав наночастиц PEG может отрицательно повлиять на эффективность трансфекции и увеличить иммуногенность при повторном введение комплексов наночастиц с нуклеиновой кислотой. Данный эффект обусловлен выработкой антител против PEG, которые ускоряют выведение наночастиц из организма и способствуют появлению побочных реакций из-за нарушения биораспределения [25]. Наличие PEG в составе наночастиц также приводит к ограничению во взаимодействии с клеточными мембранами. Для решения данной дилеммы были предложены расщепляемые PEG-липидные комплексы, которые “сбрасываются” с поверхности наночастиц при воздействии условий клеточного микроокружения (например, восстановительных условий, pH или ферментативной активности), что позволяет мембране наночастицы и клеточной мембране взаимодействовать для дальнейшей интернализации внутрь клетки [25]. PEG является критически важным и клинически подтвержденным компонентом в нескольких одобренных FDA генотерапевтических препаратах и препаратах на основе РНК, особенно в составах LNP для доставки РНК. В том же вышеупомянутом препарате Патисиран липид в составе липидных наночастиц модифицирован PEG. Аналогичная модификация липидных компонентов в составе липидных наночастиц присутствует и в других одобренных FDA генотерапевтических препаратах – вакцинах против COVID-19 Комирнати (BNT162b2) от «Pfizer-BioNTech» и Spikevax (мРНК-1273) от «Moderna» [89].
1.2.2. Биодеградируемые полимеры Учитывая, что для ГТ часто необходимо повторное введение препарата и предпочтительна сниженная цитотоксичность, биоразлагаемые полимерные векторы, как синтетические, так и природные, имеют явное преимущество перед небиоразлагаемыми. Синтетические полимеры обладают превосходной универсальностью химической структуры и стабильностью в производстве, но они могут обладать недостатками в плане взаимодействия с клетками. Напротив, природные полимеры обладают высокой биосовместимостью, но имеют проблемы в промышленном производстве из-за разницы в происхождения исходного сырья.
1.2.2.1. Полилактид (PLA) Полилактиды – гомополимеры молочной кислоты (PLA, англ. polylactic acid) и ее сополимеры с гликолевой кислотой (PLGA, англ. poly(lactide-coglycolide) acid), а также полиалкилцианоакрилаты (PACA, англ. poly(alkylcyanoacrylates)) являются примерами относительно безопасных (малотоксичных) синтетических полимеров, подходящих для создания наносомальных лекарственных форм вследствие их биосовместимости и способности к деградации в организме. PLA представляет собой синтетический биоразлагаемый полимер, широко применяемый для доставки лекарственных средств. Остаток карбоновой кислоты в составе полимера in vivo гидролизуется в молочную кислоту и быстро превращается в глюкозу, выводимую из организма без выраженных побочных эффектов. В настоящее время PLA вызывает интерес с точки зрения разработки частиц для целевой доставки, что возможно посредством различных модификаций структуры носителя. В многочисленных исследованиях показана перспективность применения наночастиц на основе биосовместимых и биодеградируемых полимеров, таких как сополимеры молочной и гликолевой кислот (PLA / PLGA), как систем доставки широкого спектра противоопухолевых веществ, антибиотиков, антисептиков, противовоспалительных веществ, антиоксидантов, белков и нуклеиновых кислот. Сополимер молочной и гликолевой кислот (PLGA) используется в составе многих одобренных FDA лекарственных препаратов с модифицированным высвобождением, среди которых микросферы (Vivitrol®, Lupron Depot®, Sandostatine LAR®, Risperdal Consta®, Trelstar®, Bydureon®) и имплантаты in situ (Eligard®, Sublocade®). Сополимеры молочной и гликолевой кислот отличаются низкой токсичностью, высокой биосовместимостью и способностью к биодеградации, что обуславливает их широкое применение при разработке систем адресной доставки и депо-форм. В некоторых исследованиях in vivo наночастицы PLGA применяли в качестве трансмукозальных наноносителей ДНК. Наночастицы на основе полилактидов имеют способность преодолевать барьер слизистой оболочки носа и транспортировать связанную модельную ДНК-вакцину [90]. В другом исследовании также использовали наночастицы PLGA в качестве систем доставки генов для восстановления и регенерации хряща. Наночастицы PLGA опосредовали доставку pDNA-SOX9 в мезенхимальные стволовые клетки человека (hMSC) и стимулировали хондрогенез у самок мышей с помощью модели подкожной имплантации [91]. Авторы ряда исследований также утверждают, что наночастицы PLGA могут легко защищать нуклеиновые кислоты от разрушения, обеспечивая контролируемое высвобождение нуклеиновой кислоты в цитоплазме, что приводит к экспрессии генов, которая может поддерживаться более месяца. Наночастицы PLGA способны инкапсулировать большие (плазмидные ДНК) и малые (миРНК) нуклеиновые кислоты; однако короткие олигонуклеотиды часто демонстрируют кинетику взрывного высвобождения, что может привести к нецелевой доставке in vivo. Однако, все еще нет одобренных FDA генотерапевтических препаратов на основе PLA или PLGA. Также химическая модификация молекул PLGA все еще является сложной задачей [92].
1.2.2.2. Хитозан (CS) Хитозан (CS) представляет собой линейный полисахарид и один из наиболее распространенных природных углеводных полимеров; он отличается биоразлагаемостью, высокими показателями биосовместимости и низкой токсичностью. Хитозан является производным хитина – вторым по распространенности в мире природным полимером после целлюлозы. Получают хитозан путем деацетилирования хитина гидроксидами при высоких температурах. Поскольку pKa хитозана 6.5, он растворим только в кислой среде, когда большинство аминогрупп протонируются с образованием комплекса с генетическим материалом. На химические свойства хитозана влияет степень деацетилирования молекулы - соотношение двух звеньев в составе молекулы: D-глюкозамина и N-ацетил-D-глюкозамина, соединенных 1,4-гликозидными связями. Растворимость хитозана в водно-кислых средах увеличивается при достижении показателя степени деацетилирования в 50%, так как при этом происходит протонирование аминогрупп, благодаря чему молекула хитозана приобретает катионные свойства. Хитозан, обладая рядом благоприятных свойств, является перспективным носителем для генетического материала. Однако его применение в нативной форме ограничено низкой растворимостью в физиологических условиях, что стимулировало разработку модифицированных производных с улучшенными характеристиками [93]. Наибольший интерес представляет гидрофильная модификация, поскольку она значительно увеличивает растворимость полимера. Одним из наиболее распространенных методов является PEGилирование – ковалентное присоединение PEG к хитозановой матрице. Однако, как уже было упомянуто ранее, модификация с помощью молекулы PEG может ухудшить эффективность трансфекции и вызвать иммунный ответ при повторном введении наночастиц. Поэтому появились подходы с альтернативными модификациями хитозана. При четвертичном аммониевым замещении гидроксильной группы получается производное хитозана – N,N,N-триметилхитозан (TMC), который проявляет высокую растворимость в широком диапазоне pH и имеет повышенный положительный заряд, усиливающий взаимодействие с клеточными мембранами и, соответственно, трансфекционную эффективность [94, 95]. Улучшенная система доставки на основе TMC, модифицированная карбоксиметилдекстраном (TMC-CMD), менее подвержена агрегации и обладает более высокой эффективность трансфекции – более 70% в in vitro экспериментах [96]. Растворимость хитозана в водной среде можно повысить, образуя соли как с органическими, так и с неорганическими кислотами. В нескольких исследованиях изучали влияние различных солей хитозана, таких как гидрохлорид хитозана (CHy), лактат хитозана (CL), ацетат хитозана (CAc), аспартат хитозана (CAs) и глутамат хитозана (CGl), на комплексы хитозан-ДНК и эффективность трансфекции, и было заявлено, что их можно использовать в качестве безопасных векторов для доставки генетического материала [97, 98]. По состоянию на 2025 год ни один препарат генной терапии на основе хитозана не одобрен FDA. Однако хитозан используется в клинических испытаниях для других целей (например, для заживления ран, доставки лекарственных веществ), а доклинические исследования расширяют его потенциал в генной терапии. 2. ПОДХОДЫ К ВЫБОРУ СИСТЕМ ДОСТАВКИ Большую роль в выборе систем доставки генетического материала в виде наночастиц играет их размер:
К молекулярным механизмам клеточного поглощения наночастиц относятся:
ЗАКЛЮЧЕНИЕ В последние годы ГТ переживает прорыв, делая возможным её применение в различных терапевтических областях. Отсутствие популярности в клинических исследованиях у невирусных комплексов для доставки генетического материала объясняется, скорее всего, их низкой эффективностью трансфекции и, в некоторых случаях, выраженной токсичностью. Так, например, в случае поликатионных конструкций неизбежно появление “дилеммы”, связанной с наличием положительного заряда. Одними из преимуществ невирусных систем доставки является их высокая нагрузочная способность, легкость синтеза и высокая модификационная пластичность, что позволяет в некоторых случаях устранить проблему токсичности. Среди невирусных систем доставки в клинических исследованиях многие конструкции представлены в виде сополимеров, модифицированных другими соединениями наночастиц. Примеры препаратов невирусной генной терапии, дошедших до клинических исследований, представлены в Дополнительных материалах. Прогресс в области развития невирусных систем доставки генетического материала в качестве многообещающих препаратов кажется медленным из-за присущей многим из данных систем токсичности, не менее выраженной, чем у вирусных векторов, и низкой эффективности трансфекции. Однако, это проблема отсутствия хорошо разработанных рецептур по созданию оптимального невирусного комплекса и недостаток в исследовательской базе знаний о детальных механизмах трансфекции данных комплексов и экспрессии генов. Возможность осуществления модификации невирусных систем позволяет обрести многообещающий потенциал, в частности, в области онкологии, вакцинации и легочных заболеваний. Мы считаем, что новые рационально разработанные невирусные векторы лишатся недостатков в отношении стабильности в организме, токсичности и эффективного высвобождения нуклеиновых кислот с дальнейшей экспрессией генов. В конечном итоге такие усилия будут способствовать продвижению перспективных кандидатов к клиническим разработкам и расширят область применения генной терапии. СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ Работа не связана с исследованиями, в которых в качестве объекта выступают люди или животные. ФИНАНСИРОВАНИЕ Исследование поддержано грантом Российского научного фонда №19-75-30007п (https:// rscf.ru/project/19-75-30007 ) КОНФЛИКТ ИНТЕРЕСОВ Авторы заявляют об отсутствии конфликта интересов. К данной статье приложены дополнительные материалы, свободно доступные в электронной версии (http://dx.doi.org/10.18097/BMCRM00287) на сайте журнала. ЛИТЕРАТУРА
|