|
Сравнительный анализ экспериментальной фармакокинетики новых нейротропных пептидных лекарственных средств
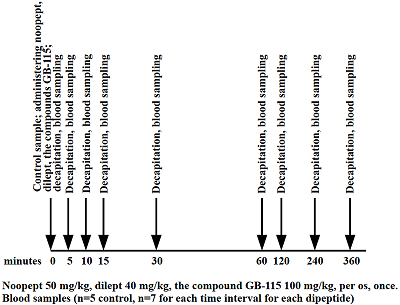
Научно-исследовательский институт фармакологии имени В.В. Закусова, Ключевые слова: нейротропные пептидные ЛС; сравнительная экспериментальная фармакокинетика; метаболизм пептидных соединений DOI: 10.18097/BMCRM00092 ВВЕДЕНИЕ Доклинические исследования фармакокинетики и метаболизма новых перспективных лекарственных средств (ЛС) являются необходимым этапом при их создании и внедрении в медицинскую практику и должны быть проведены не менее чем на 2-х видах экспериментальных животных [1]. В НИИ фармакологии имени В.В. Закусова разработаны 3 нейротропных лекарственных препарата на основе аналогов природных нейропептидов, превосходящие по нейротропной активности прототипы. Ноопепт – этиловый эфир N-фенилацетил-L-пролил-L-глицина – пептидный аналог вазопрессина и пирацетама, улучшающий нарушенные когнитивные функции, возникающие при различных нейропсихических заболеваниях, и обладающий свойствами нейропротектора, внедрен в медицинскую практику в качестве ноотропного средства; дилепт – метиловый эфир N-капроил-L-пролил-L-тирозина – дипептидный аналог природного нейропептида ангиотензина – антипсихотик с положительным мнемотропным действием прошел I фазу клинического изучения, селективный анксиолитик соединение ГБ-115 – амид N-фенил-гексаноил-L-глицил-L-триптофана, для которого завершается клиническое изучение и решается вопрос о его внедрении в клиническую практику в качестве анксиолитика для лечения фобий и тревожных расстройств. Целью настоящей работы было изучение их фармакокинетики и метаболизма при введении крысам и кроликам. МЕТОДИКА Фармакокинетику указанных лекарственных веществ (ЛВ) изучали у животных после перорального однократного введения этих субстанций. Регламент эксперимента – подбор животных, введение субстанций, пробоподготовка, количественное определение, условия хромато-масс-спектрометрического определения, статистическая обработка полученных результатов, расчет основных фармакокинетических параметров – был разработан ранее и представлен в работах: для ноопепта [2, 3], для дилепта [4, 5], для соединения ГБ-115 [6-8]. Дизайн экспериментов представлен на рисунках 1 и 2. В эксперименте на крысах использовано 5 контрольных животных, которым вводили дистиллированную воду и по 7 животных для каждого временного интервала после введения каждого изучаемого дипептида. Для кроликов использовали по 6 животных для каждого изучаемого дипептида, у которых предварительно отбирали контрольный образец крови из ушной вены, затем вводили субстанции изучаемых препаратов. Исследования фармакокинетики и метаболизма изучаемых соединений проводили на беспородных белых крысах-самцах массой 180-220 г и кроликах-самцах породы шиншилла массой 3,0-3,5 кг. Субстанции препаратов вводили крысам зондом перорально в дозе 50 мг/кг для ноопепта, 40 мг/кг – для дилепта и 100 мг/кг для соединения ГБ-115. Кроликам субстанции препаратов вводили в дозах: для ноопепта – 50 мг/кг, дилепта – 40 мг, соединения ГБ-115 – 33 мг/кг. Дизайн экспериментов представлен на рисунке 1 (крысы) и рисунке 2 (кролики). Крыс декапитировали через 5, 10, 15, 30, 60 мин и 2, 4, 6 ч после введения препаратов. У кроликов отбор крови проводили из ушной вены с помощью катетера через 15, 30, 60 мин и 2, 4, 6 ч после введения субстанций изучаемых соединений. Затем проводили экстракцию изучаемых соединений из плазмы крови крыс и кроликов и их количественное определение, как представлено в вышеуказанных работах. В данной работе в сравнительном аспекте анализируются результаты проведенных доклинических исследований фармакокинетики и метаболизма этих препаратов у крыс и кроликов, связанные не только со структурными особенностями изучаемых соединений, но и межвидовыми различиями энзиматических систем ЖКТ используемых экспериментальных животных.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ В результате проведенных исследований фармакокинетики ноопепта было установлено, что препарат в неизмененном виде определяется в плазме крови крыс в течение 25-30 мин после введения субстанции, что значительно больше по сравнению с природными нейропептидами [9-11]. При этом он быстро и интенсивно метаболизируется с образованием 3-х основных метаболитов: N-фенилацетил-пролил-L-глицина, N-фенилацетил-пролина и цикло-пролил-L-глицина (ЦПГ) (рис. 3). Было установлено, что ЦПГ обнаруживается не только в плазме, но и мозге крыс и так же, как исходное соединение, обладает сходной фармакологической активностью [12].
В таблице 1 представлены фармакокинетические параметры ноопепта и ЦПГ после перорального введения крысам субстанции ноопепта, из которой следует, что фармакокинетические параметры, характеризующие стадию абсорбции ноопепта и поступления неизмененного препарата и его метаболита в системный кровоток – величины максимальной концентрации и времени ее достижения (Сmax и Tmax) – различаются незначительно: величина Сmax для метаболита ниже на 12%, а Tmax - по сравнению с аналогичными параметрами для ноопепта; но затем, на стадии распределения и элиминации фармакокинетические параметры – площадь под фармакокинетической кривой (AUC), период полувыведения (T1/2), среднее время удержания (MRT) ЦПГ - многократно выше по сравнению с аналогичными параметрами ноопепта.
Таким образом, метаболит ЦПГ быстро обнаруживается в плазме крови крыс, его площадь под фармакокинетической кривой значительно превосходит величину этого параметра у ноопепта, что указывает на его большую устойчивость к энзиматическим системам ЖКТ крыс. Метаболит намного медленнее элиминирует из плазмы крови крыс по сравнению с ноопептом и лучше распределяется во внутренней среде организма, о чем свидетельствует его значительно большая величина MRT. После перорального введения субстанции дипептида дилепта крысам концентрация препарата в системном кровотоке ниже чем при введении ноопепта, однако дилепт определяется в плазме крыс более продолжительное время (в течение 1 ч) после введения [3, 4], как по сравнению с ноопептом, так и по сравнению со своим природным прототипом – нейротензином, период полувыведения которого составляет 2-5 мин [10]. Дилепт подвергается интенсивной биотрансформации с образованием 2-х основных продуктов метаболизма: М-1 – N-капроил-L-пролил-L-тирозина и М-2 – N-капроил-L-пролина. При этом метаболит М-1 обладает собственной фармакологической активностью [13]. Активный метаболит М-1 определяется в плазме крови крыс в более высокой концентрации и более продолжительное время (в течение 4-6 ч) по сравнению с неизмененным препаратом, который определяется в плазме крови крыс в течение 1 ч после перорального введения субстанции. Основные фармакокинетические параметры дилепта и его активного метаболита М-1 у крыс, представленные в таблице 1, позволяют сделать заключение о том, что низкая величина Cmax дилепта в плазме крови крыс и небольшая величина AUC отражают невысокую абсолютную биодоступность дилепта после перорального введения субстанции в сравнении с внутривенным введением, которая составляет 0.1% [4, 5]. Это связано не только с интенсивным пресистемным метаболизмом препарата, но и с его быстрой элиминацией из сосудистого русла и хорошим распределением во внутриклеточном пространстве организма крыс [14]. После перорального введения крысам соединения ГБ-115 – аналога холецистокинина-4, изучаемое соединение быстро всасывается из ЖКТ и поступает в системный кровоток, достигает Cmax через 15 мин после введения, определяется в системном кровотоке в течение 1 ч после введения, что значительно превосходит T1/2 своего прототипа – холецистокинина-4, период полувыведения которого составляет несколько минут [11]. Значение величины MRT свидетельствует о быстром и интенсивном распределении препарата из центрального кровотока в периферические органы и ткани крыс. Метаболитов соединения ГБ-115 в условиях нашего эксперимента обнаружено не было. При сравнении фармакокинетических параметров ноопепта, дилепта и соединения ГБ-115 у крыс следует отметить, что наблюдаются различия на всех стадиях их фармакокинетики. Так, на стадии абсорбции лучше всего всасывается ноопепт, на что указывают более высокое значение величины Cmax и низкое Tmax по сравнению с аналогичными параметрами других изучаемых дипептидов. Отличаются и параметры, характеризующие процессы метаболизма и выведения изучаемых ЛВ. Дилепт более интенсивно метаболизируется, чем ноопепт, концентрация его активного метаболита М-1 значительно превышает концентрацию исходного соединения. Анксиолитик ГБ-115 не подвергается метаболическому превращению, что, по-видимому, связано с его менее выраженной пресистемной элиминацией, он занимает промежуточное положение между ноопептом и дилептом по параметрам, характеризующим стадию абсорбции. Кроме того, у этого дипептида значительно больше величина MRT, что свидетельствует о его лучшем распределении в организме крыс по сравнению с эфирными производными дипептидов – ноопептом и дилептом. Подводя итог данному этапу исследования следует отметить, что различия фармакокинетических параметров 3-х изучаемых дипептидов, полученные на крысах, связаны со структурными особенностями изучаемых соединений, в первую очередь, с различным составом аминокислот, определяющим их фармакологическую активность, обусловливающим полярность и заряд изучаемых соединений, и заместителями, придающими липофильность молекулам дипептидов, которая увеличивается от ноопепта – ацетильная группа, затем – дилепт – капроильный радикал и, наконец, соединение ГБ-115, в структуру которого входит гексаноильный фрагмент. Кроме того, следует отметить, что эфирные производные дипептидов – ноопепт и дилепт лучше всасываются в ЖКТ, но в то же время более подвержены более выраженному энзиматическому воздействию, по сравнению с амидом которым является соединение ГБ-115. Это согласуется с данными, полученными при изучении другого дипептидного эфира ациклавира [14]. Основные фармакокинетические параметры изучаемых соединений после перорального введения их субстанций кроликам представлены в таблице 2.
Из таблицы 2 видно, что ноопепт у кроликов лучше и быстрее всасывается, особенно по сравнению с дилептом, о чем свидетельствует различие величин Cmax, Tmax, и AUC по сравнению с аналогичными параметрами 2-х других дипептидов, что, очевидно, связано не только с их структурными различиями, но и с активностью энзиматических систем, принимающих участие в метаболизме изучаемых дипептидов. Ноопепт также быстрее элиминирует из плазмы крови кроликов по сравнению с дилептом и соединением ГБ-115, на что указывает значительное различие величин периода полувыведения, что свидетельствует о быстром и лучшем перераспределении ноопепта из плазмы крови кроликов во внутренней среде организма этих животных. Метаболизм дилепта в организме кроликов также выражен в значительно меньшей степени, чем у крыс, но метаболит М-1 определяется в достаточном количестве для оценки его фармакокинетики. При изучении фармакокинетики соединения ГБ-115 было установлено, что на стадии абсорбции, характеризующейся параметрами Сmax и Тmax, он занимает промежуточное положение между ноопептом и дилептом, а на стадии элиминации анксиолитик по соответствующим фармакокинетическим параметрам (T1/2, MRT) ближе к дилепту. В организме кроликов медленнее происходят процессы как абсорбции дипептидов, так и процессы метаболизма под влиянием ферментов ЖКТ, что согласуется с литературными данными о том, что активность эстераз снижается в ряду крыса > кролик > собака > человек [15]. На это же указывает более продолжительный период полувыведения изучаемых соединений у кроликов. Таким образом, анализируя результаты проведенных исследований, следует отметить, что фармакокинетика пептидных ЛВ зависит не только от структурных особенностей и физико-химических свойств субстанций изучаемых соединений, но и активности энзиматических систем, принимающих участие в их пресистемном метаболизме и, по-видимому, в большой степени зависит от скорости систем активного транспорта пептидных соединений через мембраны ЖКТ, а также печеночного и почечного кровотока экспериментальных животных [16- 18]. ЗАКЛЮЧЕНИЕ Установлены различия фармакокинетики у крыс трех дипептидных нейротропных препаратов, которые связаны не только со структурными особенностями этих дипептидов, но и с различной интенсивностью процессов их метаболизма у этих экспериментальных животных. Соединение ГБ-115, представляющее собой амид дипептида, более устойчиво к ферментативной деградации по сравнению с эфирными производными дипептидов – ноопептом и дилептом. У кроликов отмечено усиление абсорбции изучаемых дипептидов по сравнению с их абсорбцией у крыс, что сопровождалось увеличением их максимальных концентраций и величин площадей под фармакокинетическими кривыми. Кроме того, наблюдался более медленный метаболизм этих соединений и вследствие этого увеличение продолжительности пребывания исследуемых пептидных соединений в неизмененном виде в плазме крови кроликов по сравнению с крысами. Полученные данные о межвидовых различиях фармакокинетики имеют важное значение при прогнозировании фармакокинетики новых пептидных соединений у человека и разработке их эффективного и безопасного применения в клинике. СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ Эксперименты одобрены этическим комитетом НИИ фармакологии имени В.В.Закусова. ЛИТЕРАТУРА
|